哈兽研在H7N9病毒适应哺乳动物宿主机制研究取得进展
时间:2019-06-26
来源:哈兽研
2019年6月18日,美国微生物学会(ASM)旗下顶级刊物mBio在线发表了中国农业科学院哈尔滨兽医研究所国家禽流感参考实验室题为“Low polymerase activity attributed to PA drives the acquisition of the PB2 E627K mutation of H7N9 avian influenza virus in mammals”的研究成果,研究团队在H7N9禽流感病毒适应哺乳动物宿主机制研究方面取得重要进展,揭示了H7N9禽流感病毒PA蛋白所导致的病毒在哺乳动物细胞上的低聚合酶活性是使其在小鼠体内复制过程中发生PB2/E627K突变的内在驱动力。

自2013年H7N9流感病毒在我国出现后,目前已造成1568人感染,死亡率接近40%。禽流感病毒需要获得哺乳动物适应性突变后才能在人体内有效地复制和传播。早在1993年,美国科学家就发现流感病毒在哺乳动物细胞中复制时会在病毒聚合酶蛋白PB2上发生E627K突变,但该突变产生的机制26年来一直是未解之谜。
1.不同禽流感病毒在MDCK细胞和小鼠中获得PB2 E627K突变的能力不同。
研究团队前期发现PB2/E627K突变是H7N9流感病毒对人致病力增强的关键,同时该突变增加H7N9病毒在人之间的传播能力。为了研究H7N9和H9N2在哺乳动物宿主复制过程中是否具有相同的获得PB2 E627K突变的能力,研究者首先选择了1株H7N9禽流感病毒株A/pigeon/Shanghai/S1421/2013[PG/S1421(H7N9)和5株H9N2禽流感病毒株在MDCK细胞中传代。结果发现不同禽流感病毒在MDCK细胞和小鼠复制过程中获得PB2 E627K突变的能力不同(表1)。

2. PA的低聚合酶活性导致了哺乳动物适应性PB2 E627K突变的出现。
在此基础上,研究团队以PG/S1421(H7N9)作为骨架下构建了一系列重组及突变病毒,每个重组病毒包含一个来自CK/5(H9N2)的基因片段,将获得的系列重组病毒感染小鼠,结合小鼠体内的病毒复制情况以及测序分析以便监测其PB2/E627K突变发生情况,结果发现,只有当PG/S1421(H7N9)的PA替换成H9N2的PA基因时,小鼠体内分离得到的病毒才会出现PB2/E627K突变(图1)。进一步的,研究揭示了H7N9禽流感病毒PA蛋白所导致的病毒在哺乳动物细胞上的低聚合酶活性是使其在小鼠体内复制过程中发生PB2/E627K突变的内在驱动力。

图1.PA基因低聚合酶活性驱动了其在小鼠体内发生PB2 E627K突变
3. PA基因N端的4个氨基酸残基对其在小鼠体内发生PB2 E627K突变P起着重要的调节作用
为了探索介导H7N9流感病毒PB2 E627K突变的PG/S1421(H7N9) PA的特异结构域,研究者构建了两个PA嵌合体,其中PG/S1421(H7N9) PA的结构域1-252或253-716被CK/5(H9N2) PA取代(图2A)。包含CK/5(H9N2) PA结构域1-252的RNP组合(在293T细胞中,7PB27PB179(1–252)PA7NP的聚合酶活性明显高于7PB27PB17PA7NP,而含有CK/5(H9N2) PA结构域253-716的RNP组合(即, 7PB27PB179(253-716)PA7NP与7PB27PB17PA7NP一样低(图2B)。小鼠体内感染研究结果显示,含有CK/5(H9N2) PA结构域1-252的嵌合PA病毒在小鼠中复制,但未获得PB2 E627K突变;相比之下,CK/5(H9N2) PA的嵌合型PA病毒在小鼠复制过程中获得了PB2 E627K突变(图2C)。这些结果表明,在H7N9病毒在哺乳动物宿主复制过程中,PA (PAN)的N端1-252结构域在介导PB2 E627K取代的获得过程中起关键作用。
进一步的,研究者以PG/S1421(H7N9) 构建了另外四个PA嵌合体,分别嵌合了CK/5(H9N2) PA的1-60、1-86、1-120、1-191,以确定PAN中决定PB2 E627K突变发生的关键区域。研究发现,PG/S1421(H7N9)和CK/5(H9N2)的PA蛋白在在121-191区仅存在142r、147V、171V和182l四个残基的差异,四种残基组合增加的聚合酶活性最大。更换四个PA残留物(142K, 147I, 171I,和182M)PG / S1421 (H7N9)与CK / 5 (H9N2) (142 R, 147V、171V和182l)可提高聚合酶活性能够消除其在小鼠获得PB2 E627K突变。以A/chicken/Guangdong/SD008/2017 [CK/ SD008(H7N9)]。此外,研究发现,这四个残基142K、147I、171I和182M在不同亚型AIVs的PA蛋白中高度保守,这表明它们在哺乳动物AIVs的适应性中可能具有广泛的作用。
图2.PA基因N端的4个氨基酸残基对其在小鼠体内发生PB2 E627K突变P起着重要的调节作用
图3 嵌合或突变体PA替代H7N9 PA可增强A549细胞病毒基因组的转录和复制
4.PA蛋白决定H7N9禽流感病毒在哺乳动物细胞上的聚合酶活性和复制依赖于宿主因子ANP32A
另一方面,本研究还发现H7N9禽流感病毒在哺乳动物细胞上的复制能力高度依赖于宿主因子ANP32A蛋白的表达,当Anp32a基因在小鼠体内被敲除后则使H7N9病毒在复制过程中失去了获得PB2/E627K突变的能力,而采取了另外一种适应哺乳动物宿主的方式,即获得PB2/D701N突变。
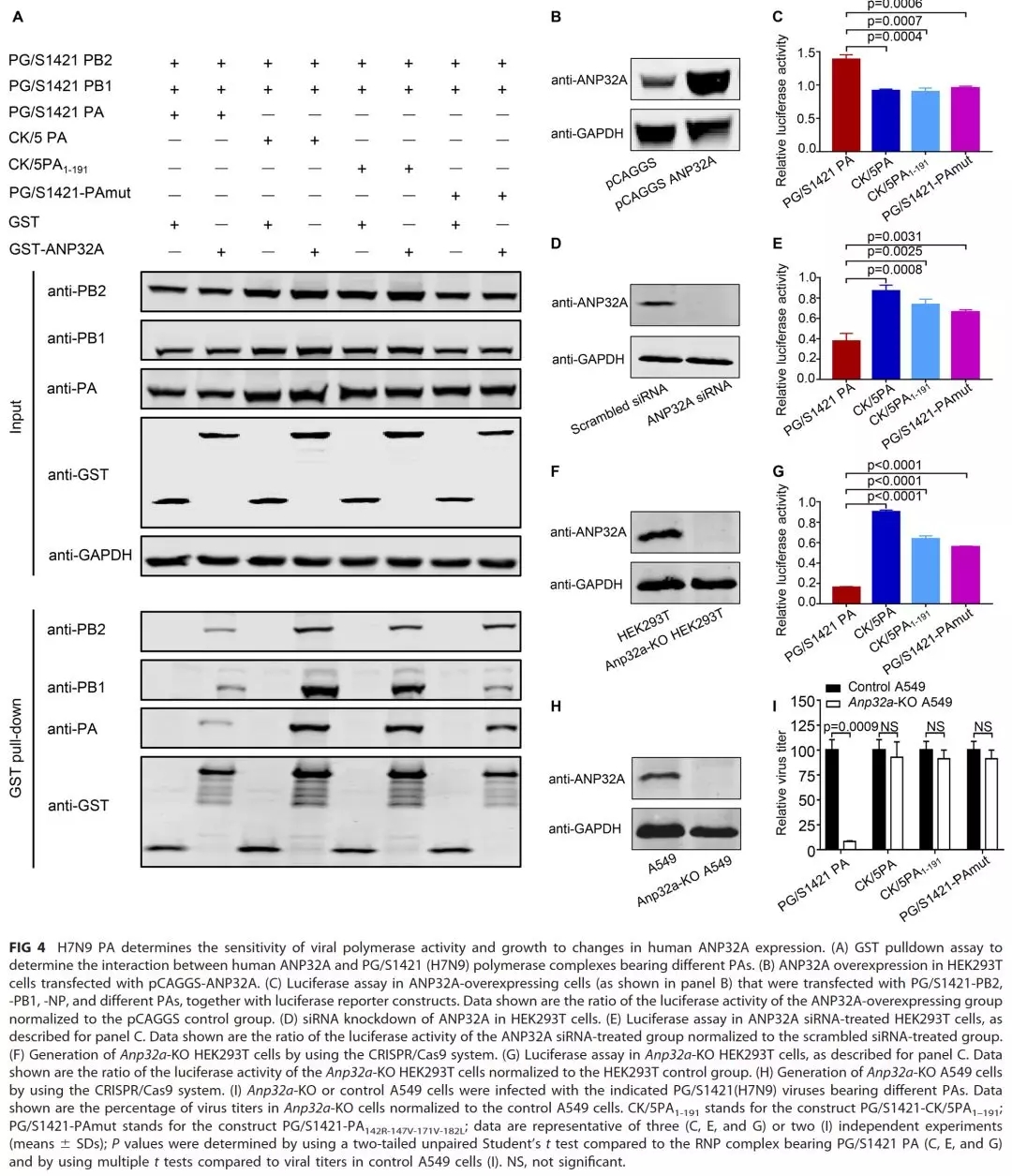
图4.PA蛋白决定H7N9禽流感病毒在哺乳动物细胞上的聚合酶活性和复制依赖于宿主因子ANP32A
该研究从病毒本身“内因”及宿主“外因”两方面,深入阐释了H7N9禽流感病毒感染人后迅速获得PB2/E627K突变而导致病毒对人类宿主适应能力和致病力增强的分子机制,从而为深入理解禽流感病毒如何适应哺乳动物宿主及跨种感染和传播这一重要科学问题做出了贡献。
陈化兰院士团队梁立滨博士、姜丽研究员为文章共同第一作者,本研究得到了国家重点研发计划(2016YFD0500205)、国家自然科学基金优秀青年科学基金(31422054)和国家自然科学基金创新研究群体(31521005)等项目资助。
ABSTRACT
Avian influenzaviruses (AIVs) must acquire mammalian-adaptive mutations before they canefficiently replicate in and transmit among humans. The PB2 E627K mutation is known to play a prominent role in the mammalian adaptation of AIVs. The H7N9 AIVs that emerged in 2013 in China easily acquired the PB2 E627K mutation upon replication in humans. Here, we generate a series of reassortant or mutant H7N9 AIVs and test them in mice. We show that the low polymerase activity attributed to the viral PA protein is the intrinsic driving force behind the emergence ofPB2 E627K during H7N9 AIV replication in mice. Four residues in the N-terminal region of PA are critical in mediating the PB2 E627K acquisition. Notably, due to the identity of viral PA protein, the polymerase activity and growth of H7N9 AIV are highly sensitive to changes in expression levels of human ANP32A protein. Furthermore, the impaired viral polymerase activity of H7N9 AIV caused by the depletion of ANP32A led to reduced virus replication in Anp32a−/− mice, abolishing the acquisition of the PB2 E627K mutation and instead driving the virus to acquire the alternative PB2 D701N mutation. Taken together, our findings show that the emergence of the PB2 E627K mutation of H7N9 AIV is driven by the intrinsic low polymerase activity conferred by the viral PA protein, which also involves the engagement of mammalian ANP32A.
1、凡注明为其它媒体来源的信息,均为转载自其它媒体,转载并不代表本网赞同其观点,也不代表本网对其真实性负责。
2、您若对该内容有疑问,请即与本网联系,本网将迅速给您回应并做处理。
3、本网站将尽力保证服务的及时性、客观性,但不保证服务一定能满足用户的要求,也不保证服务不会受中断。本网站所提供的所有信息和数据服务仅限于用户参考,不对用户的商业运作做任何具体性指导。用户因参考本网站提供的信息所带来的一切风险及法律后果由用户自行承担。